La Gazette du Canada, Partie I, volume 151, numéro 48 : Règlement modifiant le Règlement sur les médicaments brevetés
Le 2 décembre 2017
Fondement législatif
Loi sur les brevets
Ministère responsable
Ministère de la Santé
RÉSUMÉ DE L'ÉTUDE D'IMPACT DE LA RÉGLEMENTATION
(Ce résumé ne fait pas partie du Règlement.)
Résumé
Enjeux : Le Conseil d'examen du prix des médicaments brevetés (« CEPMB » ou « le Conseil ») applique un cadre réglementaire qui ne lui permet pas à l'heure actuelle de s'acquitter adéquatement de son mandat, à savoir de protéger les consommateurs canadiens contre les prix excessifs de médicaments brevetés. Au Canada, les prix des médicaments brevetés se classent parmi les plus élevés au monde et, malgré d'importants changements dans le marché des médicaments, le Règlement sur les médicaments brevetés n'a pratiquement pas été modifié depuis plus de 20 ans. Il faut moderniser le Règlement afin de donner au CEPMB des outils réglementaires plus pertinents et plus efficaces et ainsi, mieux protéger les Canadiens contre les prix excessifs des médicaments brevetés.
Description : La présente proposition aurait pour effet de modifier le Règlement sur les médicaments brevetés (le « Règlement ») de sorte que le cadre réglementaire du CEPMB inclue de nouveaux facteurs de réglementation du prix et des dispositions sur la production de rapports faisant état de renseignements sur les prix pratiqués par les titulaires de brevets qui permettront au CEPMB de protéger les consommateurs canadiens contre les prix excessifs. La proposition comporte cinq éléments.
Nouveaux facteurs de réglementation du prix en vertu de la réglementation et mise à jour de l'annexe des pays de comparaison
(1) Doter le CEPMB de trois nouveaux facteurs de réglementation du prix lui permettant d'examiner le prix d'un médicament breveté à l'aune de sa valeur pour les patients et de son incidence sur le système de soins de santé.
(2) Actualiser l'annexe au Règlement qui mentionne les pays (ci-après le CEPMB7) où les titulaires de brevets produisent des rapports qui comportent des renseignements sur l'établissement des prix de sorte à inclure des pays dont les priorités en matière de protection des consommateurs, la richesse économique et les médicaments commercialisés sont comparables à ceux du Canada. Cela permettrait au CEPMB d'obtenir des données nécessaires pour réglementer les prix qui se fondent sur des comparaisons correspondant davantage au mandat du CEPMB et aux priorités du Canada quant aux politiques nationales.
Nouvelles dispositions en matière de rapports
(3) Alléger les obligations en matière de rapports dans le cas des médicaments brevetés à usage vétérinaire, des médicaments en vente libre brevetés et des médicaments « génériques » brevetés, c'est-à-dire ceux dont la vente est autorisée par la ministre de la Santé au moyen d'une présentation abrégée de drogue nouvelle (PADN). Comme ces produits posent un risque moindre de s'imposer sur le marché et de se vendre à des prix excessifs, cela permettrait au CEPMB de concentrer ses efforts sur les médicaments qui posent un risque plus élevé de se vendre à des prix excessifs.
(4) Modifier les obligations imposées aux titulaires de brevets de produire des rapports sur les renseignements sur les prix de sorte à inclure les nouveaux facteurs.
(5) Exiger des titulaires de brevets de produire des rapports sur les prix et les recettes nets de tout rajustement de prix, comme des rabais ou des remises consentis directement ou indirectement à de tierces parties. Cela garantirait que le CEPMB est très bien informé des prix réels des médicaments brevetés au Canada et assurerait une amélioration de la pertinence et de l'incidence des comparaisons des prix au pays.
Énoncé des coûts et avantages : Les modifications proposées entraîneraient des avantages nets pour les Canadiens estimés à 12,6 milliards de dollars (valeur actualisée nette) sur 10 ans en raison de la réduction des prix des médicaments brevetés. Des prix plus bas diminueraient les pressions financières sur les assureurs publics et privés et amélioreraient l'accès à prix abordable pour les Canadiens qui paient de leur propre poche. Le manque à gagner pour l'industrie est évalué à 8,6 milliards de dollars (valeur actualisée) sur 10 ans. Les coûts pour l'industrie sont estimés à 9 000 $ par année en tout, incluant les coûts d'administration et de conformité. Les coûts pour le gouvernement d'environ 8,8 millions de dollars par année (valeur actualisée) incluraient une augmentation du personnel et des ressources du CEPMB en prévision de la multiplication des activités de conformité et d'application de la loi.
On ne prévoit pas que ces modifications généreront des incidences négatives sur l'emploi dans le secteur d'activité ni sur les investissements au Canada. Lorsque le cadre réglementaire en vigueur a d'abord été pensé il y a de cela 30 ans, les décideurs politiques étaient d'avis que la protection conférée par les brevets de même que le prix étaient des facteurs clés de l'investissement en recherche et développement (R-D) dans l'industrie pharmaceutique, mais les faits ne permettent pas de confirmer cette relation. Le niveau des investissements en R-D de l'industrie par rapport aux ventes effectuées par les titulaires de brevets au Canada recule depuis la fin des années 1990 et, de nos jours, a atteint un creux historique, même si les prix pratiqués au Canada sont les plus élevés au monde. Les présentes modifications viseraient à harmoniser les prix pratiqués au Canada avec ceux de pays qui, malgré des prix plus bas, bénéficient d'investissements plus élevés dans leur secteur pharmaceutique.
Règle du « un pour un » et lentille des petites entreprises : La règle du « un pour un » s'applique et le fardeau administratif prévu est estimé à 3 062 dollars (en dollars de 2012) par année. La lentille des petites entreprises ne s'applique pas.
Coordination et coopération à l'échelle nationale et internationale : La réglementation des prix des médicaments est une pratique courante dans le monde, même si les approches varient beaucoup. Ces différences s'expliquent souvent par la nécessité d'adapter les instruments de politique de sorte à fonctionner dans le cadre du système de soins de santé de chaque pays. Bien que les pays surveillent ce qui se fait à l'étranger sur le plan des modèles, c'est davantage pour se tenir au courant des pratiques exemplaires dans le monde que par souci d'harmonisation. La réglementation du prix des médicaments brevetés afin d'empêcher qu'ils soient excessifs ne fait pas l'objet de dispositions régissant le commerce.
Contexte
Les médicaments brevetés sont une partie importante du système de soins de santé du Canada
Les médicaments brevetés permettent de prévenir des maladies et d'en guérir, en plus de sauver des vies. Mais quant aux dépenses en médicaments sur ordonnance et aux résultats qu'ils méritent, les Canadiens n'en ont pas pour leur argent. Les dépenses en médicaments au Canada ont augmenté de moins de 10 % des dépenses totales en santé au moment de mettre en place le régime d'assurance maladie il y a 49 ans, à environ 16 % de nos jours. Les médicaments forment maintenant la seconde catégorie la plus importante de dépenses en soins de santé, devant les soins médicaux et après les frais d'hospitalisation (ce qui comprend les médicaments administrés à l'hôpital). Les Canadiens dépensent plus en médicaments par habitant que tout autre pays dans le monde, exception faite des États-Unis. Des dépenses plus importantes en médicaments peuvent compliquer l'accès à des médicaments novateurs en exerçant une pression sur l'enveloppe budgétaire destinée aux médicaments des assureurs publics et privés, peuvent imposer un fardeau financier aux patients qui paient leurs médicaments de leurs propres deniers et peuvent signifier moins de ressources dans d'autres domaines essentiels au bon fonctionnement du système de soins de santé.
En janvier 2016, les ministres fédéraux, provinciaux et territoriaux se sont mis d'accord pour travailler ensemble à améliorer l'accessibilité, l'abordabilité et l'usage approprié des médicaments afin de mieux satisfaire aux besoins du système de soins de santé. Le gouvernement du Canada est déterminé à s'acquitter de cette tâche et prend des mesures pour réduire le coût des médicaments, pour accélérer l'accès à de nouveaux médicaments sécuritaires et efficaces, et pour appuyer le développement d'outils permettant de mieux encadrer les pratiques de prescription. Afin d'appuyer ces mesures, le budget fédéral de 2017 prévoit un investissement de 140,3 millions de dollars sur cinq ans, à compter de l'exercice 2017-2018, et de 18,2 millions de dollars au cours des exercices suivants. Les modifications réglementaires proposées contribuent à cette initiative du point de vue du prix des médicaments brevetés.
Le Conseil d'examen du prix des médicaments brevetés (« CEPMB » ou « le Conseil »)
Le CEPMB a été créé en 1987 pour être le « pilier » de la protection des consommateurs dans le cadre d'un ensemble important de réformes apportées à la Loi sur les brevets (« la Loi »), visant à encourager des investissements plus importants en R-D dans le domaine de la pharmacologie au Canada en resserrant la protection des brevets. La Loi prévoit une période au cours de laquelle le titulaire du brevet d'un médicament perçoit les droits exclusifs accordés en vertu de ce brevet. En vertu de la Loi, le CEPMB est un organisme doté de pouvoirs quasi judiciaires dont le mandat réglementaire consiste à veiller à ce que le titulaire de brevet n'abuse pas des droits de son brevet en facturant au consommateur un prix excessif au cours de cette période de monopole de droit.
Ensemble, la Loi et le Règlement sur les médicaments brevetés (le Règlement) forment le cadre réglementaire des prix des médicaments brevetés du CEPMB. Les règlements qui concernent les prix des médicaments brevetés et l'information au sujet de ceux-ci sont établis sur recommandation de la ministre; cependant, le CEPMB exécute son mandat de réglementation en toute indépendance vis-à-vis de la ministre.
La Loi sur les brevets et le Règlement sur les médicaments brevetés
Bien que le cadre réglementaire ne fasse aucunement mention d'une définition de ce qui est « excessif », il précise toutefois les facteurs et les renseignements dont le Conseil doit tenir compte pour déterminer si un prix est excessif. Voici les facteurs réglementaires actuels de fixation du prix comme ils sont établis à l'article 85 de la Loi :
- le prix de vente du médicament sur un tel marché;
- le prix de vente de médicaments de la même catégorie thérapeutique sur un tel marché;
- le prix de vente du médicament et d'autres médicaments de la même catégorie thérapeutique à l'étranger;
- les variations de l'indice des prix à la consommation.
Le Règlement précise les renseignements sur les prix que le titulaire du brevet doit déclarer au CEPMB afin que celui-ci puisse fixer les prix et rendre compte sur les tendances. Il comprend des obligations de déclarer l'information relative à l'identité et au prix des médicaments brevetés vendus au Canada et leurs prix dans sept pays étrangers où ils sont également vendus. Actuellement, les sept pays mentionnés à l'annexe du Règlement (le CEPMB7) sont les États-Unis, le Royaume-Uni, la France, l'Allemagne, la Suisse, l'Italie et la Suède. Bien que l'article 85 de la Loi permette d'ajouter au Règlement d'autres facteurs de réglementation du prix à appliquer, jusqu'à maintenant, aucun facteur n'a été proposé à des fins d'études.
Compendium des politiques, des lignes directrices et des procédures du CEPMB
Un certain nombre des principaux concepts de réglementation dans la Loi et le Règlement ont été précisés dans des lignes directrices et opérationnalisés au moyen de celles-ci. Le CEPMB est autorisé à formuler des lignes directrices non contraignantes en vertu de l'article 96 de la Loi, sous réserve d'une consultation auprès des intervenants concernés. La finalité des lignes directrices consiste à établir les politiques et les procédures mises en œuvre par le personnel du Conseil pour recenser les médicaments dont le prix pourrait être excessif et à tenir les titulaires des brevets généralement au courant de ces mêmes politiques et procédures.
Modalités de fonctionnement du cadre réglementaire actuel
En vertu du cadre réglementaire actuel du CEPMB, mis en œuvre par l'entremise des lignes directrices, un nouveau médicament breveté est évalué en fonction des bienfaits thérapeutiques qu'il procure par comparaison avec les médicaments déjà sur le marché. Selon le résultat de ce processus, le CEPMB fixe un prix plafond pour les nouveaux médicaments brevetés qui repose sur le prix médian de ce même médicament dans les pays du CEPMB7, sur le prix le plus élevé d'un médicament appartenant à la même catégorie thérapeutique et vendu au Canada, ou encore sur une combinaison des deux. Une fois qu'un titulaire de brevet a fixé un prix de lancement pour la mise sur le marché d'un médicament en tenant compte du prix plafond, le CEPMB permet des hausses annuelles de son prix suivant l'indice des prix à la consommation (IPC), à la condition que ces hausses ne fassent pas en sorte que le prix au Canada soit supérieur au prix le plus élevé du même médicament dans les pays du CEPMB7.
Le cadre réglementaire actuel du CEPMB est opérationnalisé par le personnel du Conseil qui ouvre une enquête sur les médicaments dont le prix semble excessif. Le personnel du Conseil applique les tests et les seuils indiqués dans les lignes directrices à chacun des médicaments brevetés vendus au Canada, informe le titulaire du brevet qu'il fait l'objet d'une enquête si les prix échouent à ces tests et à ces seuils et tente de s'entendre avec le titulaire du brevet pour qu'il prenne un engagement de conformité volontaire (ECV) en fonction du niveau du prix conforme décrit dans les lignes directrices. Un ECV est un document rédigé par le titulaire d'un brevet l'engageant à se conformer aux lignes directrices du CEPMB, y compris à rajuster le prix du médicament breveté en question à un niveau conforme aux lignes directrices et à accorder une compensation pour d'éventuelles recettes excessives qui pourraient avoir été perçues après avoir vendu le médicament breveté à un prix non conforme aux lignes directrices au Canada.
Si un ECV acceptable n'est pas conclu, le cas est porté en audience publique contradictoire devant un panel composé de membres du Conseil. Au cours d'une audience, le panel du Conseil agit en qualité d'arbitre neutre entre les parties (le personnel du Conseil et le titulaire du brevet). Le panel du Conseil doit tenir compte de chacun des facteurs indiqués au paragraphe 85(1) au moment de déterminer si le prix d'un médicament en vente au Canada est excessif. Le panel du Conseil n'est pas lié par les lignes directrices lors d'une audience, bien que le personnel du Conseil, au moment de présenter la preuve devant le Conseil, s'appuie souvent sur des tests et des méthodes que l'on retrouve dans les lignes directrices pour démontrer que le médicament a été vendu à un prix excessif. Si le panel du Conseil conclut que le médicament a été vendu à un prix excessif, il peut émettre une ordonnance visant à obliger le titulaire du brevet à appliquer un prix non excessif et à lui ordonner de rembourser les trop-perçus découlant de la vente du médicament à un prix excessif. Une ordonnance émise par le Conseil peut être appliquée de la même façon qu'une ordonnance de la Cour fédérale.
L'évolution du marché et la hausse des coûts des médicaments au Canada
Depuis la mise sur pied du CEPMB il y a maintenant 30 ans, le marché des médicaments a passablement changé. Le développement de la médecine est de plus en plus axé sur des médicaments dont les coûts sont plus élevés, comme dans le cas des produits biologiques, des thérapies génétiques qui s'adressent à des populations de patients plus restreintes, ainsi que des médicaments prescrits pour des maladies rares. Le risque d'affirmer son pouvoir sur le marché en appliquant une pratique de prix excessifs est souvent plus élevé dans le cas de ces produits, car il y a peu ou pas de produits de substitution et le titulaire du brevet n'a pas à faire face à la concurrence. Cela est particulièrement vrai des médicaments qui sont les premiers de leur catégorie ou lorsque les médicaments de rechange sont moins efficaces ou ont des effets secondaires moins tolérables.
La dynamique actuelle des marchés a contribué à une hausse importante des prix des médicaments au Canada; faute d'y répondre, la situation se maintiendra. Entre 2005 et 2016, le nombre de médicaments au Canada dont le coût de traitement annuel par patient est d'au moins 10 000 $ a augmenté de 20 à 135. Cela représente entre 30 et 40 % des nouveaux médicaments brevetés qui s'ajoutent chaque année aux médicaments qui relèvent de la compétence du CEPMB; il s'agit d'une hausse remarquable dans ces catégories de médicaments au cours d'un bref laps de temps. En 2015, 20 médicaments représentaient un coût de traitement annuel par patient de plus de 50 000 $. De nos jours, les médicaments de spécialité dont le coût est élevé représentent près du quart des coûts assumés par les assureurs publics et privés, mais moins de 1 % de leurs bénéficiaires.
Au Canada, les prix des médicaments brevetés se classent parmi les plus élevés au monde. Sur les 35 États membres de l'Organisation de coopération et de développement économiques (OCDE), seuls les États-Unis et le Mexique affichent des prix de médicaments brevetés plus élevés que le Canada. En 2015, les prix médians de l'OCDE pour les médicaments brevetés étaient en moyenne de 22 % inférieurs à ceux pratiqués au Canada.
Rajustements de prix consentis de manière confidentielle
De plus en plus, les fabricants de produits pharmaceutiques négocient avec les assureurs des rajustements de prix en échange du remboursement de leurs produits par les régimes d'assurance. Ces rajustements de prix sont habituellement négociés discrètement, avec entente qu'ils ne seront pas rendus publics. Cela signifie qu'il y a un écart croissant entre la liste des prix publics et les prix plus bas réellement payés sur le marché en raison du recours plus fréquent à des rajustements consentis de manière confidentielle.
Limites de la réglementation actuelle en matière de prix
Au cours des 20 dernières années, de nombreux pays qui établissent des prix plafonds pour les médicaments se sont appuyés sur la comparaison des prix pratiqués dans d'autres pays. Compte tenu de l'émergence de médicaments plus chers, associée aux rajustements de prix consentis de manière confidentielle, certains pays ont dû se moderniser en adoptant de nouvelles méthodes qui, dans le cas de tels médicaments, reposent davantage sur l'évaluation de la valeur économique d'un nouveau médicament par rapport à leur système de santé respectif, et moins sur la comparaison des prix des médicaments à l'échelle internationale. Entre 2010 et 2012, 23 pays européens ont commencé à planifier et à exécuter des réformes majeures de leur cadre réglementaire pour les prix des médicaments brevetés. Bien que la comparaison des prix internationaux soit encore amplement appliquée en matière de réglementation des prix dans le monde, on l'utilise de plus en plus souvent en tant que complément à d'autres facteurs de détermination des prix.
Facteurs de réglementation du prix
L'article 85 de la Loi établit les facteurs de réglementation des prix dont le Conseil doit tenir compte au moment de décider si un médicament est, ou a été, vendu à un prix excessif au Canada. Les facteurs actuels de fixation du prix incitent le Conseil à prendre en considération le prix de vente du médicament ou d'autres médicaments de la même catégorie thérapeutique pratiqué à l'étranger. Le CEPMB s'en remet aux prix publics au moment de comparer les prix dans d'autres pays; toutefois, ces prix publics ne tiennent pas compte des rajustements de prix négociés de manière confidentielle avec certains assureurs, pratique devenue systémique au Canada et ailleurs dans le monde. À une époque caractérisée par le coût élevé des médicaments spécialisés, la part des rajustements de prix négociés de manière confidentielle peut s'avérer importante. Cela signifie qu'il y a un écart croissant entre la liste des prix publics et les prix plus bas réellement payés sur le marché et fait en sorte que le CEPMB doit réglementer en se fondant sur des prix publics qui correspondent de moins en moins à ce que les assureurs paient vraiment sur le marché. Le CEPMB a besoin d'autres facteurs qu'il pourra utiliser pour évaluer si un prix est excessif.
L'annexe des pays de comparaison
L'annexe au Règlement indique les sept pays pour lesquels le titulaire d'un brevet doit présenter des renseignements sur les prix pratiqués. Le CEPMB se base sur les prix des mêmes médicaments brevetés dans ces pays, lorsque cela est possible, pour établir les prix plafonds des médicaments au moment de les commercialiser au Canada et au cours des années qui suivent. La liste des pays à l'annexe du Règlement n'a pas été actualisée depuis qu'elle a été établie il y a 30 ans de cela. À cette époque, les décideurs en matière de politiques étaient convaincus que la protection conférée par les brevets et le prix étaient des facteurs clés de l'investissement en R-D dans l'industrie pharmaceutique. On a donc décidé d'offrir un niveau de protection conférée par un brevet et de prix pour les médicaments comparable à celui d'autres pays ayant une industrie pharmaceutique forte parce qu'on croyait que le Canada finirait par profiter de niveaux comparables de R-D. Toutefois, le pourcentage des dépenses en R-D par rapport aux recettes que les titulaires de brevets tirent de la vente de leurs médicaments au Canada recule depuis la fin des années 1990 et est actuellement inférieur à ce que l'on observait au Canada au moment des réformes de la Loi sur les brevets de 1987. À titre de comparaison, et malgré le fait que le Canada fait partie des pays appliquant les prix de médicaments brevetés les plus élevés, l'investissement en R-D de l'industrie par rapport aux ventes dans les pays du CEPMB7 atteint une moyenne de 22,8 % par rapport à 4,4 % au Canada. Par conséquent, aucune donnée probante ne permet de confirmer l'existence d'un lien déterminant entre les prix pratiqués dans un pays et le lieu de l'investissement en R-D de l'industrie. D'autres facteurs, tels que l'emplacement du siège social, l'infrastructure des essais cliniques ainsi que les groupes scientifiques, semblent constituer des déterminants beaucoup plus influents en ce qui concerne l'endroit où les investissements pharmaceutiques se font dans une économie mondiale.
L'intention stratégique du choix initial de l'annexe ne s'est pas concrétisée et n'est plus considérée comme le fondement le plus adéquat pour la compilation des pays mentionnés à l'annexe. L'obligation réglementaire imposée aux titulaires de brevets de déclarer les prix pratiqués dans le CEPMB7 fait en sorte que les prix au Canada des médicaments brevetés demeurent parmi les plus élevés au monde.
Enjeux
Le Conseil détermine si un prix est excessif en se fondant sur les facteurs de réglementation du prix contenus dans la Loi ainsi que sur les dispositions sur la production de rapports faisant état de renseignements sur les prix pratiqués par les titulaires de brevets qui sont précisées dans le Règlement. L'évolution du secteur des médicaments à l'échelle canadienne et mondiale a fait ressortir deux limites importantes de l'actuel cadre réglementaire du Conseil : (1) l'inefficacité des facteurs de réglementation du prix courants lorsqu'il s'agit d'étoffer adéquatement l'évaluation que fait le CEPMB du caractère excessif; (2) la nature insuffisante des exigences en matière de production de rapports sur l'information relative aux prix appliqués par les titulaires de brevets.
En vertu de l'actuel cadre réglementaire, le caractère excessif est évalué presque exclusivement en fonction des listes de prix publics au Canada et à l'étranger. Cette réalité est problématique en raison de l'arrivée de médicaments spécialisés très onéreux et des prix courants qui ne se comparent pas à ce que les assureurs publics et privés paient réellement. Voici les principales limites du cadre actuel :
- Le cadre n'offre pas de facteurs de réglementation du prix supplémentaires autres que la comparaison des prix et l'IPC permettant au CEPMB de déterminer si un prix est excessif. Il ne vérifie pas si le prix d'un médicament tient compte des éléments suivants :
- la valeur d'un médicament pour un patient : les médicaments qui offrent des avantages cliniques considérables aux patients ou qui sont les seuls de leur classe thérapeutique feront l'objet d'une plus grande demande que les médicaments qui ne sont que légèrement meilleurs que la norme de soins ou qui ne sont qu'un parmi tant d'autres de leur classe;
- le nombre de patients pouvant profiter du médicament : la taille d'un marché pour un médicament peut avoir des répercussions sur son prix attendu et la capacité de payer d'un pays donné pour obtenir ce médicament;
- la richesse d'un pays : les pays possédant des ressources économiques plus abondantes peuvent se permettre d'acquérir plus de médicaments ou des médicaments plus chers que des pays possédant moins de ressources.
- La liste de pays servant de points de comparaison des prix (CEPMB7) n'est pas à jour. Les prix des nouveaux médicaments au Canada sont comparés à ceux appliqués dans des pays où les médicaments sont chers et non à ceux de pays comparables du point de vue du marché des médicaments, de la protection des consommateurs et de la richesse. Le choix des pays peut donc avoir des conséquences importantes sur les prix plafonds des médicaments brevetés au Canada. Comme le CEPMB se sert de comparaisons de prix à l'échelle internationale, l'utilisation de l'ensemble de pays de comparaison CEPMB7 a pour effet de permettre l'établissement de prix plus élevés au Canada que ce que l'on retrouverait autrement si le marché des médicaments des pays de comparaison ressemblait davantage au marché canadien.
Objectifs
Les modifications proposées au Règlement sur les médicaments brevetés permettraient au CEPMB de se doter de facteurs de réglementation du prix et de dispositions sur la production de rapports faisant état de renseignements sur les prix des titulaires de brevets nécessaires pour s'acquitter de son mandat, à savoir protéger les consommateurs canadiens contre les prix excessifs de médicaments brevetés. On prévoit que la mise en œuvre de ces modifications par le CEPMB entraînera une diminution des prix des médicaments brevetés au Canada de sorte qu'ils correspondent à peu de chose près à leur valeur pour les patients et pour le système de soins de santé et aux prix que les Canadiens veulent et peuvent payer.
Description
Les modifications proposées comportent cinq éléments.
Facteurs de réglementation du prix et mise à jour de l'annexe des pays de comparaison
- Présenter de nouveaux facteurs de réglementation du prix fondés sur des critères économiques qui permettraient au CEPMB de garantir des prix non excessifs qui tiennent compte de la valeur des médicaments brevetés et de la volonté et de la capacité du Canada de payer ces derniers.
- Actualiser l'annexe des pays de comparaison utilisée par le CEPMB pour comparer les prix internationaux afin de mieux tenir compte du mandat de protection des consommateurs du CEPMB et des prix médians de l'OCDE.
Dispositions en matière de production de rapports
- Alléger les obligations en matière de rapports dans le cas des médicaments brevetés à usage vétérinaire, des médicaments en vente libre brevetés et des médicaments « génériques » brevetés.
- Établir les dispositions sur la production de rapports de sorte à permettre au CEPMB d'opérationnaliser les nouveaux facteurs de réglementation des prix.
- Exiger des titulaires de brevets de produire des rapports sur les prix et les recettes nets de tout rajustement de prix intérieur, comme des remises ou des rabais directs ou indirects consentis à de tierces parties ou la distribution de biens ou de services gratuits.
Une description plus détaillée de chacune des modifications proposées suit.
1. Présenter de nouveaux facteurs de réglementation du prix fondés sur des critères économiques qui garantiraient des prix tenant compte de la valeur des médicaments brevetés et de la volonté et de la capacité du Canada de payer ces derniers
Cette proposition de modification entraînerait l'ajout de trois facteurs de réglementation du prix, soit la valeur pharmacoéconomique, la taille du marché ainsi que le produit intérieur brut (PIB) et le PIB par habitant au Canada. Ces nouveaux facteurs de réglementation du prix permettraient au CEPMB de tenir compte d'autres aspects très pertinents du caractère excessif des prix qui se rapportent à la valeur de l'avantage pour la santé produit par le médicament ainsi qu'à la volonté et à la capacité des consommateurs canadiens de payer de tels médicaments. Ces nouveaux facteurs ne s'appliqueraient qu'aux ventes de médicaments brevetés effectuées après l'entrée en vigueur des modifications proposées.
Valeur pharmacoéconomique du médicament au Canada
Le prix payé pour obtenir un médicament doit tenir compte de la valeur qu'il produit par rapport à son coût. Parallèlement, il doit également prendre en compte le coût rattaché à l'offre du médicament si le fabricant continue d'investir dans la production de nouveaux médicaments. L'évaluation pharmacoéconomique définit, mesure et compare les coûts et les avantages d'un médicament donné pour les patients et le système de santé. L'ajout de ce facteur obligerait le Conseil à vérifier que le prix du médicament est proportionnel aux avantages qu'il apporte aux patients dans le contexte du système de santé canadien.
Taille du marché pour la vente du médicament au Canada et dans d'autres pays
L'ajout de ce facteur au Règlement pourrait permettre au CEPMB d'élaborer des analyses des répercussions sur le marché pour des médicaments qui risquent de représenter un défi pour les assureurs en raison de la taille du marché du médicament. La conséquence de l'établissement d'un prix excessif dépend à la fois du prix et du volume; plus le marché du médicament est grand au Canada, plus la conséquence sur son prix est importante. Lorsque les assureurs publics et privés sont appelés à couvrir le coût d'un médicament pour un nombre important de patients, le coût élevé d'un médicament peut faire en sorte que les personnes qui en ont besoin n'aient pas les moyens de se le procurer. Les prix canadiens pourraient être évalués en fonction des prix internationaux et des niveaux de prévalence (nombre de personnes atteintes de la maladie) afin d'évaluer la relation prix-volume et de produire une analyse raisonnable des répercussions sur le marché. L'ajout du facteur de la taille du marché permettrait également au CEPMB de réévaluer les prix des médicaments brevetés au fil du temps. Une fois le médicament offert sur le marché, le titulaire de brevet peut demander une approbation réglementaire auprès de Santé Canada afin que le médicament puisse être utilisé pour traiter d'autres problèmes de santé ou prescrit par des médecins pour une utilisation hors indication (c'est-à-dire prescrit afin de traiter des problèmes de santé pour lesquels le médicament n'a pas reçu d'approbation réglementaire). Puisque les médicaments brevetés sont protégés contre l'arrivée de nouveaux médicaments sur le marché, il se peut que les fluctuations ultérieures de la taille du marché où ils peuvent être vendus n'aient pas de conséquences sur les prix. Puisqu'on présume que les titulaires de brevets établissent leurs prix de lancement à un niveau profitable pour récupérer leurs investissements initiaux, une croissance de la taille du marché devrait harmoniser et ajuster les prix à la baisse à un niveau comparable. Le défaut de le faire pourrait laisser entendre que le prix original, pour un marché élargi, est désormais excessif.
PIB au Canada et PIB par habitant au Canada
Le PIB constitue une mesure de la production économique d'un pays. La croissance du PIB mesure à quel point la valeur du marché rajustée en fonction de l'inflation des biens et des services produits par une économie augmente avec le temps. Le PIB par habitant mesure la capacité de production d'un pays relativement à sa population. Dans ce contexte, la croissance du PIB canadien peut constituer un indicateur de la capacité du pays à payer année après année, alors que le PIB par habitant est un indicateur du pouvoir d'achat des particuliers. En ajoutant le facteur de fixation du prix PIB au Canada et PIB par habitant au Canada, le CEPMB disposerait de mesures de la capacité de payer des médicaments à l'échelle nationale et individuelle. L'ajout de ce facteur permettrait au CEPMB d'évaluer l'incidence du prix d'un médicament sur les finances des consommateurs et des assureurs. Il pourrait également permettre au CEPMB d'élaborer des analyses de répercussions sur le marché pour des médicaments qui risquent de représenter un défi sur le plan de l'abordabilité pour les assureurs en raison de la taille du marché du médicament.
2. Actualiser l'annexe des pays de comparaison utilisée par le CEPMB pour comparer les prix internationaux afin de mieux tenir compte du mandat de protection des consommateurs du CEPMB et des prix médians de l'OCDE
Le CEPMB utilise les listes de prix publics des médicaments brevetés vendus dans les pays du CEPMB7 pour fixer les prix plafonds de ces mêmes médicaments brevetés au Canada lorsqu'ils arrivent sur le marché et au cours des années suivantes. Selon les niveaux de prix, le choix des pays peut avoir des conséquences importantes sur les prix plafonds des médicaments brevetés au Canada.
La modification proposée demande de réexaminer la composition du CEPMB7 pour mettre à jour la liste des pays à l'annexe et s'assurer d'y inscrire des pays qui cadrent mieux avec le mandat de protection du consommateur du CEPMB ainsi qu'avec le niveau de richesse et la situation du Canada en tant que marché important pour la vente de médicaments. La liste des pays pris en compte pour l'annexe révisée regroupait les 35 pays de l'OCDE puisque ces pays appliquent les mêmes politiques économiques et sociales que le Canada. On n'a pas jugé nécessaire d'obliger les titulaires de brevets à produire des rapports sur les prix dans l'ensemble des 35 pays membres pour les raisons suivantes : (1) le fardeau en matière de production de rapports serait important; (2) certains pays de l'OCDE se comparent davantage au Canada en ce qui a trait aux priorités stratégiques et à la situation économique; (3) il pourrait s'avérer difficile d'obtenir de l'information sur les prix et les ventes de la part de certains pays. Trois critères ont été utilisés pour sélectionner un sous-ensemble de pays de l'OCDE qui composera l'annexe révisée.
Premièrement, les pays doivent avoir mis en place des politiques d'établissement du prix des médicaments qui s'harmonisent bien avec le mandat de protection du consommateur du CEPMB, notamment avoir adopté des mesures de restriction nationales d'établissement de prix pour protéger les consommateurs contre les prix élevés des médicaments. À titre d'exemple, les États-Unis ne satisfont pas à ce critère.
Deuxièmement, les pays doivent posséder des ressources économiques raisonnablement comparables à celles du Canada, notamment une situation économique comparable à celle du Canada, selon la mesure du PIB par habitant. On s'assure ainsi que les prix concordent avec la capacité de payer des Canadiens pour obtenir des médicaments. Par exemple, le PIB par habitant du Canada se classe au 11e rang parmi les pays de l'OCDE, mais le prix des médicaments brevetés arrive au 3e rang. L'annexe proposée regroupe des pays qui présentent un PIB par habitant raisonnablement supérieur, comparable ou inférieur à celui du Canada.
Troisièmement, les pays doivent présenter des caractéristiques de la taille du marché des médicaments comparables à celles du Canada, telles que la population, la consommation, les revenus et l'arrivée sur le marché de nouveaux produits. Ainsi, les marchés de taille comparable qui en résultent produisent un niveau de prix proportionnel à la part canadienne des ventes de médicaments à l'échelle mondiale.
En fonction de ces critères, on propose d'inclure les pays suivants dans l'annexe : l'Australie, la Belgique, la France, l'Allemagne, l'Italie, le Japon, les Pays-Bas, la Norvège, la Corée du Sud, l'Espagne, la Suède et le Royaume-Uni (CEPMB12). Si l'on inscrivait un plus grand nombre de pays à l'annexe, les tests de prix seraient moins sensibles à l'influence exercée par les pays où les prix sont élevés ou bas; par ailleurs, on atténuerait les conséquences lorsque la présentation de l'information sur les prix et les ventes est retardée ou qu'une telle information n'est pas disponible. Par exemple, avec uniquement sept pays de référence, si seulement deux de ces pays ne fournissent pas ou fournissent en retard l'information relative aux prix, l'incidence sur la médiane de l'échantillon peut atteindre 10 %. En faisant passer l'annexe à 12 pays, l'incidence est réduite à seulement 2 %. En utilisant une liste légèrement plus longue, le CEPMB obtiendrait une perspective plus équilibrée des prix courants sur le marché ainsi qu'une médiane de l'échantillon plus stable sans imposer de dispositions en matière de production de rapports beaucoup plus strictes aux titulaires de brevets ni un fardeau administratif plus lourd au CEPMB.
3. Alléger les obligations en matière de rapports dans le cas des médicaments brevetés à usage vétérinaire, des médicaments en vente libre brevetés et des médicaments « génériques » brevetés
Dans sa version actuelle, le Règlement exige seulement que des rapports sur les prix et les ventes de médicaments brevetés à usage vétérinaire et de médicaments en vente libre brevetés (c'est-à-dire les médicaments qui ne contiennent pas de substances contrôlées ou qui ne sont pas des produits radiopharmaceutiques ou biologiques en vertu de la Loi sur les aliments et drogues et du Règlement sur les aliments et drogues) soient transmis au CEPMB si des plaintes ont été déposées. Les modifications proposées réduiraient encore plus les obligations en matière de production de rapports pour ces médicaments; ainsi, l'information relative aux prix, aux ventes et à l'identité ne serait fournie qu'à la demande du CEPMB dans le cas de tous les médicaments à usage vétérinaire et médicaments en vente libre, y compris les médicaments qui pourraient contenir une substance contrôlée ou qui sont des produits radiopharmaceutiques et/ou biologiques. Par ailleurs, les modifications élargiraient la portée de ces mêmes obligations réduites en matière de production de rapports de façon à inclure les médicaments génériques brevetés (soit les médicaments approuvés au moyen d'une PADN). Les titulaires de brevets pour des médicaments génériques sont généralement confrontés à une plus grande concurrence, et le risque d'établissement de prix excessifs en raison du pouvoir commercial n'est généralement pas source de préoccupation. L'objectif de ces propositions de modification est d'éviter aux titulaires de brevets un fardeau réglementaire inutile en matière de production de rapports dans le cas de médicaments qui présentent un faible risque d'établissement de prix excessifs. Ces modifications permettraient également au CEPMB de concentrer ses ressources sur des médicaments qui présentent un risque plus important d'établissement de prix excessifs.
4. Établir les dispositions sur la production par les titulaires de brevets de rapports donnant de l'information sur les prix des médicaments pour que le CEPMB puisse opérationnaliser les nouveaux facteurs de réglementation des prix
Le règlement actuel précise les renseignements que les titulaires de brevets doivent fournir au CEPMB concernant les facteurs de réglementation du prix courants. Les renseignements portent sur le prix des médicaments brevetés vendus au Canada et dans d'autres pays, les recettes tirées des ventes par les titulaires de brevets et les dépenses en R-D. Les titulaires de brevets seraient tenus de fournir de nouveaux renseignements au CEPMB concernant les nouveaux facteurs que sont la valeur pharmacoéconomique et la taille du marché. Les titulaires de brevets n'auraient pas à présenter de données sur le PIB et le PIB par habitant puisque Statistique Canada se chargerait de fournir cette information.
Renseignements sur la valeur pharmacoéconomique : Les titulaires de brevets seraient tenus de transmettre au CEPMB toutes les analyses coût-utilité publiées qui utilisent la valeur du point de vue du coût par année de vie pondérée par la qualité (QALY). Les analyses coût-utilité sont perçues par les experts comme étant l'approche de référence pour examiner la valeur économique de nouveaux médicaments. Le coût par QALY quantifie l'avantage en mesurant l'allongement de la vie ou l'amélioration de la qualité de vie. Il s'agit de la mesure de la valeur pharmacoéconomique la plus reconnue puisqu'elle permet de faire des comparaisons entre différents types de médicaments en utilisant la même unité de mesure. Avec l'ajout de cette exigence en matière de production de rapports, le CEPMB pourrait envisager d'introduire le concept d'un seuil maximum de coût par QALY au Canada.
En raison de la grande expertise que peuvent nécessiter la préparation et la validation de telles analyses, cette exigence se limiterait aux analyses préparées par une organisation publique canadienne, comme l'Agence canadienne des médicaments et des technologies de la santé (ACMTS) ou l'Institut national d'excellence en santé et en services sociaux (INESSS). Ces organisations possèdent une expertise spécialisée et réalisent habituellement des analyses pharmacoéconomiques dans le cas de médicaments pour lesquels une demande de remboursement par les assureurs publics a été présentée. Le CEPMB pourrait utiliser ces analyses dans le cadre de son évaluation du caractère excessif des prix. Il ne répéterait pas le travail effectué par l'ACMTS et l'INESSS dans le cadre des processus de remboursement.
Même si le nouveau facteur de valeur pharmacoéconomique ne s'appliquerait qu'aux ventes de médicaments brevetés effectuées après l'entrée en vigueur de la version modifiée du Règlement, l'obligation de soumettre la dernière analyse coût-utilité publiée serait élargie à l'ensemble des médicaments brevetés, tant ceux déjà sur le marché au moment de l'entrée en vigueur du Règlement modifié que tous les nouveaux médicaments mis en vente après la date de l'entrée en vigueur. En règle générale, on produit une analyse coût-utilité uniquement pour un médicament donné lorsque certains points critiques sont franchis dans le cycle de vie du médicament (par exemple au moment du lancement initial sur le marché ou par suite de l'approbation réglementaire aux fins de l'utilisation du médicament pour traiter un nouveau problème de santé). Même si la dernière analyse coût-utilité d'un médicament existant date de plusieurs années, elle pourrait encore contenir les données les plus récentes et pertinentes dont pourrait se servir le CEPMB au moment d'appliquer le nouveau facteur de valeur pharmacoéconomique. Les titulaires de brevets seraient tenus de fournir uniquement les analyses publiées; ils ne seraient pas obligés de préparer une analyse coût-utilité s'ils ne disposent pas déjà d'une telle analyse.
Renseignements sur la taille du marché : Les titulaires de brevets seraient tenus de fournir au CEPMB de l'information sur la consommation maximale prévue du médicament au Canada, par quantité de médicaments vendus dans sa forme posologique définitive, pour chaque forme posologique et concentration que l'on envisage de vendre. On croit que les titulaires de brevets produisent déjà de telles estimations dans le cadre de leurs plans de développement visant à faire entrer un nouveau médicament breveté sur le marché canadien. Les titulaires de brevets doivent déjà compiler ces renseignements pour la préparation de leurs plans d'activités ou pour les processus de l'ACMTS. Avant l'arrivée d'un médicament sur le marché, les titulaires de brevets se fient aux statistiques et aux renseignements disponibles sur la prévalence (nombre de personnes atteintes d'une maladie) dans un pays donné et sur l'incidence (nombre prévu de nouveaux cas chaque année) pour produire des prévisions de ventes. Ils doivent également tenir compte d'autres facteurs tels que la concurrence pour estimer la part de marché éventuelle de leur nouveau médicament.
Les titulaires de brevets devront aussi fournir au CEPMB des estimations mises à jour; par exemple, une mise à jour peut s'avérer nécessaire lorsqu'un médicament est approuvé par Santé Canada pour traiter un nouveau problème de santé, ce qui vient élargir le marché qui était prévu pour ce médicament. Le nouveau facteur relatif à la taille du marché s'appliquerait uniquement aux ventes de médicaments brevetés effectuées après l'entrée en vigueur de la version modifiée du Règlement. Cependant, étant donné qu'il faut prévoir jusqu'à trois ans pour que le marché d'un nouveau médicament arrive à pleine maturité, les titulaires de brevets de médicaments qui sont déjà sur le marché et qui ont été mis en vente pour la première fois au plus trois ans avant l'entrée en vigueur du règlement modifié ou qui ont obtenu une approbation réglementaire aux fins de l'utilisation pour traiter un nouveau problème de santé au cours de cette même période de trois ans seraient également dans l'obligation de fournir de l'information sur la consommation maximale prévue de ces médicaments au Canada.
5. Exiger des titulaires de brevets de produire des rapports sur les prix et les recettes nets de tout rajustement de prix
Dans sa version actuelle, le Règlement exige des titulaires de brevets de fournir des renseignements concernant les rajustements de prix pour le premier point de vente seulement. Les titulaires de brevets ne sont pas tenus de déclarer les rajustements de prix majeurs qu'ils consentent peut-être à de tiers assureurs, comme les assureurs provinciaux qui remboursent le coût d'un médicament vendu à un patient. Les assureurs provinciaux comptent parmi les principaux payeurs de médicaments brevetés au Canada. S'il ne dispose pas de cette information, le CEPMB fixe le prix plafond non excessif d'un médicament en se fondant sur des données qui ne tiennent compte que de certains rajustements de prix. Cette modification obligerait les titulaires de brevets à produire des rapports sur les prix et les recettes nets de tout rajustement de prix et autre redressement, y compris des rabais, des remises, ainsi que des biens et des services gratuits, consentis à une partie qui paye ou rembourse le médicament. Même si la plupart des redressements risquent d'entraîner une diminution des prix, l'objectif de cette modification est de consigner l'information relative à tout redressement, y compris les redressements générant une hausse de prix. Ce renseignement sera considéré comme privilégié en vertu de l'article 87 de la Loi sur les brevets, et le Conseil le prendra en considération au moment de déterminer si un prix est excessif.
Grâce à cette information, le CEPMB se servirait d'un prix net de tout redressement pour calculer le prix plafond non excessif. À l'heure actuelle, le CEPMB fixe un prix non excessif pour les médicaments en se fondant sur les prix d'autres médicaments de la même classe thérapeutique qui sont vendus au Canada. Puisque l'information relative aux prix ne comprend pas les rajustements de prix consentis à de tierces parties, les prix des produits de comparaison qui arrivent ensuite sur le marché sont souvent gonflés (car les prix plafonds de ces médicaments sont fixés au moyen d'une liste de prix gonflés dans le cas des médicaments déjà en vente et non en se fondant sur le véritable prix payé au Canada). Par conséquent, les tests de comparaison des classes thérapeutiques donnent des prix plafonds supérieurs à ce que l'on obtiendrait si le prix réel payé était connu du CEPMB. Si l'on obligeait la divulgation du véritable prix, qui comprend tous les rajustements de prix accordés par le titulaire de brevet, le CEPMB pourrait inclure ces rabais dans le calcul qu'il fait du prix de vente moyen. Par ailleurs, les titulaires de brevets pourraient se servir de ce mécanisme pour se conformer au régime en calculant le véritable prix de la vente tenant compte de l'ensemble des rabais et des remises, directs et indirects.
Options réglementaires et non réglementaires considérées
Statu quo
L'option de ne pas prendre de mesures a été étudiée et écartée, car il manque au cadre réglementaire actuel du CEPMB des facteurs de réglementation du prix efficaces et des dispositions suffisantes sur la production de rapports faisant état des prix par les titulaires de brevets. Les facteurs actuels ne tiennent pas compte de tous les aspects du caractère excessif dans le cas des nouvelles catégories de médicaments qui sont apparues depuis la création du CEPMB. Les dispositions actuelles du CEPMB sur la production de rapports sur les prix par les titulaires de brevets produisent des renseignements incomplets sur l'établissement des prix sur le marché intérieur et donnent des renseignements sur les prix internationaux provenant d'un certain nombre de pays dont les prix élevés des médicaments brevetés ne se comparent pas au marché canadien.
Modernisation non réglementaire (actualisations du Compendium des politiques, des lignes directrices et des procédures du CEPMB)
Cette option se limiterait essentiellement à des tests de prix révisés qui continuent de reposer entièrement sur des méthodes de référencement aux prix intérieurs et internationaux. Cette option a été étudiée sous tous ses aspects et tient compte également d'une consultation auprès des intervenants réalisée par le CEPMB en 2016, mais a été écartée, car le simple fait d'actualiser les lignes directrices ne parvient pas à corriger les insuffisances sous-jacentes du règlement actuel. Pour obtenir tous les renseignements sur les rajustements des prix et diminuer la dépendance actuelle à l'égard du test des prix internationaux, il faut une réforme de la réglementation passant par l'ajout de nouveaux facteurs. Avec un cadre réglementaire modernisé, le CEPMB disposerait d'une base plus solide pour actualiser ses lignes directrices.
Avantages et coûts
Les avantages quantitatifs de l'énoncé des coûts et des avantages se rapportent à la diminution des dépenses globales en médicaments brevetés au Canada qui devrait entraîner une chute des prix. Les coûts quantifiés se rapportent aux éléments suivants : (1) la diminution des recettes générées par l'industrie en raison de la baisse des prix des médicaments brevetés; (2) l'incidence nette des nouvelles exigences administratives et des exigences réduites en matière de rapports imposées à l'industrie; (3) les coûts pour le gouvernement canadien de la vérification de la conformité aux modifications proposées.
L'avantage quantifié total de la baisse des prix des médicaments brevetés est estimé à 21,3 milliards de dollars (VA) sur 10 ans. Le coût quantifié total de cette proposition, y compris le manque à gagner global pour l'industrie, est estimé à 8,6 milliards de dollars (VA) sur 10 ans. Les coûts administratifs pour l'industrie et le gouvernement du Canada devraient, selon les prévisions, s'élever à environ 62 millions de dollars (VA) sur une période de 10 ans. La valeur actualisée nette (VAN) totale des modifications devrait s'établir à 12,7 milliards de dollars sur 10 ans, soit de 2019 à 2028. Un taux d'actualisation de 7 % a été appliqué dans tous les calculs de VA. L'analyse coûts-avantages complète est disponible sur demande.
Énoncé des coûts-avantages
| Année de base (Année 1) |
Dernière année (Année 10) |
Total (VA) |
Moyenne annualisée |
|
|---|---|---|---|---|
| Avantages | ||||
| Dépenses moins élevées en médicaments | 219 993 857 $ | 2 782 694 694 $ | 8 567 004 599 $ | 1 219 745 515 $ |
|
33 443 984 $ | 1 399 184 431 $ | 3 763 190 611 $ | 535 792 273 $ |
|
138 187 981 $ | 770 272 294 $ | 2 788 004 256 $ | 396 948 040 $ |
|
48 361 892 $ | 613 237 969 $ | 2 015 809 732 $ | 287 005 201 $ |
| Système de soins de santé | 425 688 113 $ | 5 384 514 233 $ | 12 722 001 829 $ | 1 811 322 089 $ |
| Avantages totaux | 645 681 970 $ | 8 167 208 927 $ | 21 289 006 428 $ | 3 031 067 604 $ |
| Coûts | ||||
| Industrie | 8 567 068 356 $ | 1 219 754 583 $ | ||
|
219 993 857 $ | 2 782 694 694 $ | 8 567 004 599 $ | 1 219 745 515 $ |
|
34 717 $ | 4 924 $ | ||
|
29 106 $ | 4 144 $ | ||
| Gouvernement | 4 981 481 $ | 8 025 361 $ | 61 716 822 $ | 8 787 064 $ |
|
3 849 215 $ | 5 680 633 $ | 43 361 629 $ | 6 173 704 $ |
|
981 481 $ | 2 025 361 $ | 16 119 394 $ | 2 295 033 $ |
|
143 085 $ | 304 667 $ | 2 131 142 $ | 303 425 $ |
|
7 700 $ | 14 700 $ | 104 657 $ | 14 900 $ |
| Coûts totaux (VA) | 8 628 785 178 $ | 1 228 541 647 $ | ||
| Avantages nets (VAN) | 12 660 221 250 $ | 1 802 525 957 $ | ||
| Incidences qualitatives | ||||
|
||||
Coûts
L'actuel cadre réglementaire contient déjà des dispositions en matière de production de rapports sur les prix imposées aux titulaires de brevets. Dans la plupart des cas, les catégories de renseignements à fournir et la fréquence de production de rapports demeureraient les mêmes. Le fardeau administratif pour l'industrie serait plus important en raison de l'obligation de faire rapport sur les nouveaux facteurs de réglementation du prix. La proposition mentionne également l'avantage que représente la diminution du fardeau administratif rattaché à certains types de médicaments (médicaments en vente libre, pour usage vétérinaire et approuvés au moyen d'une PADN qui sont brevetés), mais cette réduction ne serait pas suffisante pour compenser complètement les nouvelles dispositions en matière de rapports.
Industrie
Les coûts pour l'industrie engloberaient ce qui suit :
- Le respect des dispositions en matière de production de rapports sur les nouveaux facteurs de réglementation du prix. Les titulaires de brevets devront s'assurer de mettre l'information à jour lorsque de nouvelles analyses sont réalisées. Les coûts administratifs totaux devant être signalés en ce qui a trait aux nouveaux facteurs de réglementation du prix sont évalués à 6 175 $ par année ou 43 373 $ en VA sur 10 ans.
- Le coût de la conformité entraîné par la mise à jour des systèmes de production de rapports dans lesquels les titulaires de brevets doivent consigner l'information relative aux prix tous les six mois, cette mise à jour étant rendue nécessaire pour inclure l'annexe des pays qui est proposée; la mise à jour des prix intérieurs et des recettes nettes de l'industrie afin de tenir compte de tous les rajustements de prix. Les titulaires de brevets ont déjà mis en place des systèmes de production de rapports pour les prix intérieurs et internationaux; la proposition modifie uniquement le type d'information à déclarer. On estime que les coûts totaux associés à la conformité seront de 4 144 $ par année ou de 29 106 $ en VA sur 10 ans.
Réduction du fardeau administratif
La proposition élimine la nécessité de fournir de l'information sur l'identité et le prix au CEPMB dans le cas des médicaments génériques, pour usage vétérinaire et en vente libre qui sont brevetés, sauf si le CEPMB demande cette information. Quatre-vingt-seize médicaments (sur les 1 359 relevant du CEPMB) appartiennent à ces catégories et sont présentement visés par l'obligation de produire un rapport au CEPMB. Étant donné que la Cour d'appel fédérale vient tout juste de clarifier et de confirmer les compétences du CEPMB relativement à ces médicaments, le CEPMB ne tenait pas compte auparavant de la conformité à l'obligation de faire rapport sur ces mêmes médicaments. En supposant une conformité parfaite, la réduction du fardeau administratif devrait totaliser 8 656 $ (VA) sur 10 ans.
Manque à gagner pour l'industrie des médicaments
Le CEPMB régit uniquement les prix excessifs des médicaments brevetés au Canada. Toute réduction de prix et tout remboursement de trop-perçus découlant de la présente proposition devront faire l'objet d'un engagement de conformité volontaire (ECV) de la part du titulaire de brevet, qui s'engagera à respecter les nouveaux prix plafonds conformes, ou d'une ordonnance du Conseil faisant suite à une audience publique devant le Conseil au cours de laquelle un panel du Conseil aura déterminé que le médicament a été vendu à un prix excessif. On estime que cette proposition entraînera pour l'industrie une diminution des recettes totalisant quelque 8,6 milliards de dollars (VA) sur 10 ans en raison de l'abaissement des seuils s'appliquant aux prix plafonds non excessifs au Canada. Aux fins de la présente analyse coûts-avantages (ACA), on a calculé les recettes à l'échelle nationale pour l'ensemble des fabricants de médicaments brevetés au Canada, même si 90 % des sociétés faisant rapport au CEPMB sont des entreprises multinationales.
Gouvernement du Canada
Renforcement de la capacité du CEPMB
Les coûts pour le gouvernement engloberaient les fonds accordés au CEPMB pour engager du personnel supplémentaire afin d'accomplir les tâches suivantes : soutenir la hausse attendue dans les activités d'application de la loi; administrer les nouveaux facteurs de réglementation du prix. On s'attend à ce que l'année de référence (2018-2019), la deuxième année (2019-2020), la troisième année (2020-2021) et la quatrième année (2021-2022) coûtent respectivement 3,8 M$, 5,7 M$, 6,7 M$ et 7,7 M$. À partir de la cinquième année, les coûts pour le gouvernement devraient être de 5,7 M$ par année pour maintenir la capacité accrue du CEPMB.
Hausse du financement prenant la forme d'une affectation à but spécial
Lorsque le projet de règlement entrera en vigueur, les titulaires de brevets seront peut-être moins disposés à proposer des engagements de conformité volontaire et plus portés à insister pour obtenir une audience officielle qui pourrait s'éterniser. Le CEPMB aurait alors besoin de fonds additionnels pour son affectation à but spécial (ABS) afin de couvrir les frais liés aux services de conseillers juridiques et de témoins experts indépendants. Il se peut également que les titulaires de brevets contestent plus souvent les décisions prises en vertu du nouveau régime devant la Cour fédérale. On s'attend à ce que l'année de référence (2018-2019), la deuxième année (2019-2020), la troisième année (2020-2021) et la quatrième année (2021-2022) coûtent respectivement 1,0 M$, 1,8 M$, 2,8 M$ et 3,8 M$. À partir de la cinquième année, les coûts pour le gouvernement devraient être de 2,0 M$ par année pour maintenir le financement accru sous forme d'ABS versé au CEPMB.
Compensation des coûts pour Services publics et Approvisionnement Canada et pour Services partagés Canada
La hausse des niveaux de dotation au CEPMB entraînera également une augmentation des coûts afférents aux locaux et aux technologies de l'information (TI). En les combinant, on s'attend à ce que l'année de référence (2018-2019), la deuxième année (2019-2020), la troisième année (2020-2021) et la quatrième année (2021-2022) coûtent respectivement 151 000 $, 305 000 $, 328 000 $ et 331 000 $. À partir de la cinquième année, on s'attend à ce que les coûts pour le gouvernement soient de 319 000 $ par année pour compenser les coûts des locaux pour Services publics et Approvisionnement Canada et les coûts des services de TI pour Services partagés Canada.
Le coût total prévu pour le gouvernement du Canada serait de 61,7 millions de dollars en valeur actualisée nette sur 10 ans.
Avantages
Les avantages ont été calculés suivant la réduction attendue dans le niveau de risque pour la population que présentent les médicaments brevetés dont le prix est excessif au Canada.
Les avantages quantitatifs prévus ont été calculés en se fondant sur les dépenses globales réduites en médicaments brevetés. Les données de base concernant les prévisions de dépenses à venir (2017-2028) ont été calculées au moyen des tendances actuelles en matière de croissance et des lancements de produits prévus dans le créneau actuel des médicaments. Elles tiennent aussi compte de la perte attendue de la protection conférée par un brevet dans le cas de médicaments relevant présentement de la compétence du CEPMB. Les avantages nets totaux découlant des modifications proposées sont estimés à 25,1 milliards de dollars (VAN) sur 10 ans.
Dépenses moins élevées en médicaments brevetés
Les modifications proposées devraient entraîner une baisse des dépenses en médicaments brevetés évaluée à 8,6 milliards de dollars (VA) sur 10 ans.
On estime que ce sera l'ajout de nouveaux facteurs de réglementation du prix qui aura la plus grande incidence sur les dépenses en médicaments brevetés (3,8 milliards de dollars); suivent la révision de l'annexe (2,8 milliards de dollars) et la production de rapports sur les rajustements de prix et les redressements des ventes consentis à de tierces parties (2,0 milliards de dollars).
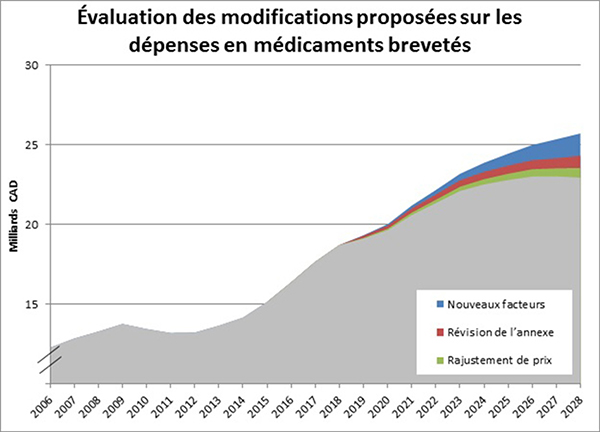
Avantages pour le système de santé
Si les modifications proposées ne sont pas apportées, on estime que les systèmes publics de santé de partout au Canada dépenseront 3,9 milliards de dollars (VA) de plus pour la même quantité de médicaments brevetés. Il s'agit d'un coût d'option intéressant pour le système public de santé au Canada puisque ces sommes pourraient être affectées à d'autres secteurs du système de santé pour mieux répondre aux besoins des Canadiens en matière de santé. Étant donné que chaque dollar dépensé dans le secteur de la santé publique a un effet d'entraînement considérable sur la santé et l'économie (voir référence 1), ce coût d'option est d'une ampleur assez importante pour le Canada. Le coût d'option total pour le système de santé rattaché au fait de payer des médicaments à un prix excessif a été estimé à 12,7 milliards de dollars (VA) sur 10 ans.
Sommaire de l'analyse de sensibilité
On a mené une analyse de sensibilité sur les deux variables qui pourraient influer fortement les conséquences estimées de la proposition. La première variable se rapporte à la mise en œuvre de la proposition par le CEPMB tandis que l'autre variable concerne le taux de croissance prévu des dépenses en médicaments brevetés. L'analyse de référence a été réalisée en supposant que le CEPMB continue d'appliquer des méthodes de test des prix qui sont comparables à celles présentement en place. Il est nécessaire de formuler une telle hypothèse puisque le CEPMB contrôle entièrement le processus de modification des lignes directrices. Par exemple, le CEPMB se sert présentement du prix médian des pays du CEPMB7 pour vérifier les prix de nouveaux médicaments par rapport à leurs prix dans d'autres pays. Le scénario de référence présume que le test du prix médian s'appliquerait également pour le nouveau groupe CEPMB12. L'analyse de sensibilité de cette variable a permis d'examiner d'autres approches possibles pour remplacer les facteurs de réglementation du prix existants ainsi que des approches possibles pour mettre en œuvre les nouveaux facteurs proposés dans les lignes directrices.
La deuxième variable concerne le taux de croissance des dépenses en médicaments brevetés. Si la croissance des dépenses en médicaments brevetés est supérieure aux prévisions, l'avantage mesuré en dollars, qui est calculé à partir d'une réduction en pourcentage s'expliquant par la baisse des prix des médicaments brevetés, sera plus grand que prévu. Dans la même veine, si la croissance dans les dépenses est inférieure aux prévisions, l'avantage global sera également moins important. Il est difficile de prévoir la croissance dans l'industrie des médicaments brevetés; l'arrivée de nouveaux types de médicaments brevetés, comme les produits biologiques, fait apparaître de nouvelles incertitudes dans les initiatives de modélisation.
L'analyse de sensibilité démontre que les dépenses totales en médicaments brevetés pourraient diminuer d'au moins 6,4 milliards de dollars (VA) après 10 ans et d'au plus 24,9 milliards de dollars (VA) après 10 ans. Dans l'analyse de sensibilité, l'incidence minimale représente la croissance des ventes de médicaments brevetés la plus faible prévue jumelée aux réformes les moins radicales apportées aux lignes directrices du CEPMB. Dans l'analyse de sensibilité, l'incidence maximale représente la croissance des ventes de médicaments brevetés la plus élevée prévue jumelée aux réformes les plus radicales apportées aux lignes directrices du CEPMB. L'actuelle ACA estime que les dépenses cumulatives de référence après 10 ans totaliseront 8,6 milliards de dollars (VA) (voir référence 2).
Sommaire de l'analyse de répartition
La grande majorité des fabricants de médicaments brevetés sont situés en Ontario, au Québec, en Colombie-Britannique et en Alberta. Ces quatre provinces comptent 98 % de l'ensemble des entreprises qui seraient touchées par les modifications proposées.
Tous les payeurs de médicaments brevetés, y compris le secteur public, le secteur privé et les particuliers de partout au pays profiteront de la baisse des prix.
Consommation selon l'âge et le sexe : Selon le rapport de Statistique Canada « Consommation de médicaments sur ordonnance chez les Canadiens de 6 à 79 ans », la consommation de médicaments sur ordonnance augmentait avec l'âge, celle-ci passant de 12 % chez les 6 à 14 ans à 83 % chez les 65 à 79 ans. La consommation de médicaments sur ordonnance était également associée à la présence de problèmes de santé physique et mentale. Le pourcentage de Canadiens consommant des médicaments sur ordonnance ne variait pas selon le revenu du ménage. Les femmes étaient généralement plus susceptibles que les hommes de déclarer prendre des médicaments sur ordonnance (47 % contre 34 %). Toutefois, chez les 6 à 14 ans, un pourcentage plus élevé de garçons que de filles consommaient des médicaments sur ordonnance, tandis que, chez les 65 à 79 ans, la prévalence de la consommation de médicaments sur ordonnance était la même pour les hommes et les femmes. L'intensité de la consommation de médicaments sur ordonnance, c'est-à-dire le nombre de médicaments différents que consomme une personne, était fortement associée à l'âge. Ainsi, de 3 % chez les 6 à 14 ans, le pourcentage de personnes prenant plus d'un médicament passait à 70 % chez les 65 à 79 ans.
Règle du « un pour un »
Le fardeau supplémentaire imposé aux titulaires de brevets par la réglementation était estimé à environ 43 373 $, auquel on soustrairait 8 656 $ en réduction estimative du fardeau de la réglementation, ce qui donne un total de 34 717 $ (valeur actualisée sur 10 ans). Ce calcul comprend les coûts initiaux de la réalisation pour le CEPMB d'analyses du rapport coût-utilité et de la taille du marché pour les médicaments qui relèvent actuellement de la compétence du CEPMB, les coûts permanents de la mise à jour de ces analyses et la réalisation pour le CEPMB d'analyses du rapport coût-utilité et d'estimations de la taille du marché pour tous les nouveaux médicaments brevetés qui sont mis sur le marché ainsi que le coût du retrait d'autres dispositions présentement en vigueur en matière de production de rapports dans le cas des médicaments brevetés à usage vétérinaire et des médicaments en vente libre et de l'ajout des médicaments génériques à ces mêmes obligations réduites en matière de production de rapports. La proposition est considérée comme une « ENTRÉE » selon la règle du « un pour un » et a une incidence estimée à 3 062 $.
| L'initiative actuelle est une : | « ENTRÉE » (règle du « un pour un ») | ||
|---|---|---|---|
| Valeurs qui doivent figurer dans le résumé de l'étude d'impact de la réglementation | Arrondissement | Unité de mesure | |
| Coûts d'administration annualisés (dollars constants de 2012) | 3 062 $ | Sans décimales | Dollars constants de 2012, année de référence pour valeur actualisée : 2012 |
| Coûts d'administration annualisés par entreprise (en dollars de 2012) | 40 $ | Sans décimales | Dollars constants de 2012, année de référence pour valeur actualisée : 2012 |
Lentille des petites entreprises
La lentille des petites entreprises ne s'applique pas aux modifications proposées, car celles-ci ne concernent que les fabricants de produits pharmaceutiques titulaires du brevet d'un médicament en vente au Canada. Sur les 77 sociétés pharmaceutiques qui relèvent de la compétence du CEPMB, aucune ne satisfait à la définition de petite entreprise. En règle générale, les médicaments brevetés sont vendus par des multinationales ou leurs filiales.
Consultation
La période de consultation pour la publication préalable dans la Partie I de la Gazette du Canada de ce projet de règlement sera de 75 jours.
Ces consultations s'appuient sur une consultation initiale menée au sujet du projet de règlement. Le 16 mai 2017, l'honorable Jane Philpott, ancienne ministre fédérale de la Santé, a annoncé le lancement de la consultation sur les modifications proposées au Règlement sur les médicaments brevetés. Un document de consultation intitulé « Protéger les Canadiens des prix excessifs des médicaments : Consultation sur les modifications proposées au Règlement sur les médicaments brevetés » a été affiché sur le site Web de Santé Canada ainsi que sur le site du gouvernement du Canada : Consultations auprès des Canadiens. L'annonce de la consultation s'est faite par voie de communiqué de presse et de courriels diffusés à l'ensemble des intervenants. De plus, conformément au paragraphe 101(2) de la Loi sur les brevets, la ministre Philpott a écrit à tous ses homologues des provinces et des territoires les invitant à lui faire part de leurs commentaires sur les modifications proposées à la réglementation. Les mémoires produits par l'ensemble des intervenants et des parties intéressées ont été acceptés jusqu'au 28 juin 2017. Au cours de cette consultation, Santé Canada a organisé neuf séances d'interaction avec des intervenants externes, y compris des représentants d'assureurs publics et privés, d'organisations de patients, du secteur pharmaceutique, des professions de la santé et du monde universitaire.
Les assureurs (publics et privés) étaient généralement favorables aux modifications proposées, affirmant que la valeur pharmacoéconomique et la taille du marché sont des facteurs très pertinents à la détermination du caractère excessif des prix. Le produit intérieur brut (PIB) comme facteur ne faisait pas l'unanimité. Les assureurs privés ont suggéré que les facteurs tiennent compte de considérations pertinentes pour les employeurs, comme l'incidence d'un médicament sur la productivité, l'absentéisme et l'indemnisation pour invalidité. Les assureurs étaient favorables à la révision de l'annexe des pays. Quoique favorables à l'allègement du fardeau découlant de la réglementation des médicaments génériques brevetés, des assureurs ont suggéré que le CEPMB continue de demander l'information sur les prix et les ventes des médicaments de cette classe qui risquent d'être vendus à un prix plus élevé. Enfin, les assureurs étaient favorables à la modification visant à ce que le CEPMB obtienne les renseignements concernant les rajustements de prix, à la condition que ces renseignements soient tenus confidentiels par le CEPMB.
Les organisations de patients ont souligné que les prix élevés des nouveaux médicaments brevetés représentent un obstacle financier à leur accès pour les Canadiens et ont demandé que la réglementation garantisse que la priorité serait donnée à la question de l'accès des patients aux médicaments. Les organisations de patients ont proposé que la réglementation prévoie une marge de manœuvre suffisante pour permettre au CEPMB de passer outre à l'indicateur coût par année de vie pondérée par la qualité (AVPQ) de sorte à tenir compte des préférences du patient et de circonstances particulières comme dans le cas des médicaments pour les maladies rares. Par ailleurs, les organisations ont demandé que l'utilisation des renseignements sur les rajustements de prix au moment de fixer le prix n'entame pas le pouvoir de négociation des assureurs.
Des représentants de l'industrie des médicaments de marque ont mentionné que les modifications proposées compliqueraient grandement la commercialisation des médicaments brevetés au Canada et ajouteraient à l'incertitude des marchés. Plusieurs ont suggéré que les facteurs économiques proposés outrepassaient le mandat du CEPMB et ont avancé qu'ils pourraient constituer un doublon inutile de l'évaluation effectuée par l'ACMTS. Ils ont fait part de leurs préoccupations concernant le fardeau réglementaire supplémentaire que représente la production de données pharmacoéconomiques et de renseignements sur l'établissement des prix à l'étranger. On a souvent proposé que les États-Unis demeurent à l'annexe des pays de comparaison. On a recommandé que le Règlement permette une approche axée sur le risque et que les dispositions concernant la production de rapports périodiques soient supprimées dans le cas des produits à faible risque. L'industrie pharmaceutique n'était pas convaincue de la manière dont le CEPMB prévoit utiliser les renseignements sur les rajustements de prix et les tenir confidentiels, mais on a laissé entendre que le fait de communiquer ces renseignements au CEPMB pourrait entraîner des rajustements de prix inférieurs pour les assureurs au Canada.
Les représentants du secteur des médicaments génériques étaient favorables à la proposition de soustraire les fabricants de médicaments génériques brevetés de l'obligation de produire périodiquement des rapports sur l'identité et le prix de ces médicaments, car ces derniers posent un faible risque d'emprise sur le marché et sont assujettis à une réglementation des prix par les provinces et les territoires. Ils ont recommandé d'étendre cette modification à d'autres formes complexes de médicaments génériques pour lesquelles Santé Canada n'émet pas de déclaration d'équivalence, comme les médicaments biosimilaires et les médicaments génériques comportant des ingrédients et des formules complexes.
Le secteur des produits de santé destinés aux consommateurs a reconnu que ses produits en vente libre sont déjà dispensés de l'obligation de fournir des rapports périodiques. Des représentants ont recommandé que la totalité des produits d'autosoins soit exemptée du cadre des médicaments brevetés, mais cela outrepasse la portée du Règlement que de modifier le champ de compétence du CEPMB en matière de médicaments brevetés.
Les représentants des associations de médecins et d'infirmières appuyaient l'utilisation de facteurs économiques pour évaluer la valeur d'un médicament, l'annexe révisée et l'obligation de produire des renseignements sur les rabais consentis de manière confidentielle au Canada. Les associations d'infirmières n'étaient pas en faveur de l'exemption des médicaments génériques brevetés des obligations en matière de production systématique de rapports. Les pharmaciens étaient favorables à l'évaluation d'un médicament en fonction de sa valeur, mais ont souligné que la valeur pharmacoéconomique devrait tenir compte des avantages et des coûts au-delà d'un indicateur AVPQ. Ils ont signalé que l'annexe des pays de comparaison devrait être révisée en fonction de la disponibilité des produits dans chacun des pays et ont demandé que la modification concernant les rajustements de prix effectués de manière confidentielle ne remette pas en cause les rajustements de prix négociés par les assureurs publics.
Les universitaires étaient favorables au facteur de valeur pharmacoéconomique proposé et à l'obligation de présenter les renseignements sur le coût par AVPQ. Certains universitaires étaient favorables à l'emploi du PIB pour déterminer un prix plafond et ont suggéré d'utiliser aussi le PIB par habitant. Les universitaires étaient moins convaincus de l'utilité des renseignements sur la taille du marché sans davantage de renseignements sur les coûts en R-D d'un médicament. La plupart d'entre eux étaient d'accord pour dire qu'il faut revoir l'annexe et retirer de la liste des pays de comparaison ceux qui n'ont pas mis en place des dispositions visant à protéger les consommateurs des prix excessifs. Les universitaires étaient généralement en faveur d'autoriser le CEPMB à recueillir des renseignements sur les rajustements de prix, bien qu'ils recommandent d'élargir le concept de rajustement des prix à tous les mécanismes de transfert auquel a recours un titulaire de brevet et qui ont une incidence sur les prix, y compris les ententes sur la rémunération au rendement; ils ont mis en garde contre l'utilisation de renseignements sur les rabais au moment de faire des comparaisons avec d'autres pays.
Les observations faites sur la réglementation ont été prises en compte lors de la rédaction de la présente proposition aux fins de publication préalable dans la Partie I de la Gazette du Canada et du résumé de l'étude d'impact de la réglementation. En particulier :
- Dans les modifications proposées, les facteurs de réglementation du prix fondés sur des critères économiques restent vagues afin de donner au CEPMB la latitude d'étudier d'autres mesures au-delà du coût par AVPQ, lorsqu'il y a lieu de le faire, et de permettre au CEPMB de mettre au point des mesures pertinentes en s'appuyant sur la taille du marché et le PIB. En tenant compte des observations reçues, le PIB par habitant s'est ajouté au facteur PIB.
- Les dispositions en matière de production de renseignements par les titulaires de brevets ont été revues de sorte à alléger autant que possible le fardeau réglementaire, tout en permettant au CEPMB d'obtenir suffisamment de renseignements pour protéger les Canadiens des prix excessifs. L'adoption des modifications proposées ne requiert pas des pays autres que le Canada de produire des analyses coût-utilité.
- Une analyse plus poussée de l'annexe telle qu'elle est proposée a été produite; une estimation des incidences sur les dépenses en médicaments brevetés est présentée dans l'analyse coûts-avantages.
- On a étudié la possibilité de supprimer les dispositions en matière de production systématique de renseignements pour les titulaires de brevets dans le cas d'autres produits à faible risque en plus des médicaments génériques brevetés. On propose que les dispositions concernant la production périodique de rapports soient supprimées dans le cas de tous les médicaments brevetés sans ordonnance, y compris les produits radiopharmaceutiques et les produits biologiques dont la vente est autorisée en vertu du Règlement sur les aliments et drogues ainsi que les médicaments contenant des substances réglementées. Bien que d'autres produits comme les médicaments biosimilaires et autres médicaments génériques brevetés qui ne sont pas autorisés par voie de PADN aient été étudiés, ces produits et leur risque de prix excessif n'ont pas pu être définis adéquatement.
- On propose que les nouvelles dispositions du Règlement en matière de production de rapports fassent état de tous les rajustements de prix qui auraient pour effet d'abaisser (comme les escomptes, les rabais, les produits gratuits et les services gratuits) ou d'élever (comme la rémunération au rendement) le prix d'un médicament.
Coopération en matière de réglementation
La présente proposition actualiserait l'annexe des pays de comparaison des prix internationaux utilisée par le CEPMB afin de mieux tenir compte du mandat de protection des consommateurs du CEPMB et des prix médians de l'OCDE; une telle harmonisation à l'échelle internationale contribuerait à une baisse du prix des médicaments au Canada.
Justification
Contrairement à la plupart des systèmes de soins de santé dans le monde, le système de soins de santé du Canada n'est pas un système à payeur unique pour les médicaments. Au Canada, les dépenses en médicaments d'ordonnance se répartissent entre assureurs publics (43 %), assureurs privés (35 %) et concitoyens qui paient de leur propre poche (22 %).
La modernisation du cadre réglementaire du CEPMB serait bénéfique pour tous ceux qui paient des médicaments au Canada en élevant la norme de protection des consommateurs. Les assureurs publics et privés du Canada bénéficieraient d'une baisse des prix plafonds de sorte que les négociations sur les prix ne se concluent plus simplement par des prix qui sont équivalents à ceux pratiqués dans d'autres pays. Les modifications permettront au CEPMB d'atteindre des prix plafonds au Canada plus près des normes internationales. Cela permettrait aux assureurs publics et privés de négocier davantage d'égal à égal avec les vendeurs, à l'image des autorités sanitaires d'autres pays. On prévoit que les cotisations aux régimes d'assurance-maladie avec participation des employeurs diminueront et que le risque que les régimes deviennent ingérables en raison de la cherté des médicaments diminuera également. Les Canadiens sans assurance qui paient de leur propre poche leurs médicaments sont ceux qui dépendent le plus du mandat de protection des consommateurs du CEPMB et qui bénéficieraient de prix plus bas pour leurs médicaments brevetés.
On estime que la présente proposition entraînera des avantages totaux pour les Canadiens de 8,6 milliards de dollars (valeur actualisée nette) au cours des 10 années suivant sa mise en œuvre.
Mise en œuvre, application et normes de service
Le règlement proposé entrerait en vigueur le 1er janvier 2019. Cela permettrait aux titulaires de brevets de se préparer à la mise en œuvre des nouveaux facteurs de réglementation du prix et des nouvelles dispositions relatives à la communication des renseignements sur les prix. La date du 1er janvier 2019 a été retenue de sorte que la mise en œuvre concorde avec les périodes de rapport du CEPMB, soit le 1er janvier et le 1er juillet. Une fois le règlement modifié publié dans la Partie II de la Gazette du Canada, les responsabilités afférentes à la mise en œuvre, à l'application et aux normes de service seraient déléguées au CEPMB. On prévoit que cela inclura la finalisation, sous la direction du CEPMB, de la consultation auprès des intervenants sur la version révisée du Compendium des politiques, des lignes directrices et des procédures qui servira à établir un consensus sur les modalités d'application du cadre révisé sous la forme de tests de prix particuliers et de validation des renseignements que transmettront les titulaires de brevets.
Les nouveaux facteurs ne régiront que les médicaments dont la vente se réalisera après l'entrée en vigueur des modifications proposées. Cependant, les dispositions du règlement modifié régissant la production de rapports seront appliquées tant dans le cas des nouveaux médicaments brevetés que des médicaments existants. Les titulaires de brevets de médicaments existants disposeraient de 30 jours suivant la date d'entrée en vigueur pour présenter une analyse coût-utilité (si possible) et de l'information sur la consommation estimative sur le marché (le cas échéant). Les renseignements sur les prix dans le cas des pays à l'annexe révisée et les renseignements sur les prix et les recettes sur le marché national qui tiennent compte des rajustements des prix devraient d'abord être communiqués dans les 30 jours suivant la fin de la période de rapport au cours de laquelle les modifications proposées entrent en vigueur (autrement dit, dans les 30 jours suivant le 30 juin 2019).
Personne-ressource
Karen Reynolds
Directrice exécutive
Bureau des stratégies de gestion des produits pharmaceutiques
Direction générale de la politique stratégique
Santé Canada
Édifice Brooke Claxton, 10e étage
70, promenade Colombine, Pré Tunney
Ottawa (Ontario)
K1A 0K9
Téléphone : 613-957-1692
Courriel : PMR-Consultations-RMB@hc-sc.gc.ca
PROJET DE RÉGLEMENTATION
Avis est donné que la gouverneure en conseil, en vertu du paragraphe 101(1) (voir référence a) de la Loi sur les brevets (voir référence b), se propose de prendre le Règlement modifiant le Règlement sur les médicaments brevetés, ci-après.
Les intéressés peuvent présenter leurs observations au sujet du projet de règlement dans les soixante-quinze jours suivant la date de publication du présent avis. Ils sont priés d'y citer la Partie I de la Gazette du Canada, ainsi que la date de publication, et d'envoyer le tout à Karen Reynolds, directrice exécutive, Bureau des stratégies de gestion des produits pharmaceutiques, Direction générale de la politique stratégique, Santé Canada, 10ème étage, édifice Brooke Claxton, 70, promenade Colombine, Pré Tunney, Ottawa (Ontario) K1A 0K9 (tél. : 613-957-1692; courriel : PMR-Consultations-RMB@hc-sc.gc.ca).
Ottawa, le 23 novembre 2017
Le greffier adjoint du Conseil privé
Jurica Čapkun
Règlement modifiant le Règlement sur les médicaments brevetés
Modifications
1 L'article 3 du Règlement sur les médicaments brevetés (voir référence 3) est modifié par adjonction, après le paragraphe (3), de ce qui suit :
(3.1) Malgré le paragraphe (3), s'agissant des médicaments ci-après, les renseignements visés au paragraphe (1) doivent être fournis au Conseil dans les trente jours suivant l'envoi, par ce dernier, d'une demande visant à ce que le breveté fournisse ces renseignements :
- a) un médicament qui n'est pas une drogue sur ordonnance au sens de l'article A.01.010 du Règlement sur les aliments et drogues;
- b) un médicament qui contient une substance désignée, au sens du paragraphe 2(1) de la Loi réglementant certaines drogues et autres substances, dont la vente ou la fourniture ne nécessite pas d'ordonnance en vertu de cette loi;
- c) un médicament à l'égard duquel un avis de conformité a été délivré d'après les renseignements et le matériel contenus dans la présentation déposée conformément à l'article C.08.002.1 du Règlement sur les aliments et drogues;
- d) un médicament destiné à l'usage vétérinaire.
2 (1) Le passage du paragraphe 4(2) du même règlement précédant l'alinéa a) est remplacé par ce qui suit :
(2) Les renseignements visés au paragraphe (1) doivent être fournis :
(2) Le paragraphe 4(3) du même règlement est remplacé par ce qui suit :
(3) Malgré le paragraphe (2), s'agissant des médicaments ci-après, les renseignements visés au paragraphe (1) doivent être fournis au Conseil pour chaque période de six mois commençant le 1er janvier et le 1er juillet de chaque année, dans les trente jours suivant l'envoi, par ce dernier, d'une demande visant à ce que le breveté fournisse ces renseignements et, au cours des deux années qui suivent la demande, dans les trente jours suivant la fin de chaque période de six mois :
- a) un médicament qui n'est pas une drogue sur ordonnance au sens de l'article A.01.010 du Règlement sur les aliments et drogues;
- b) un médicament qui contient une substance désignée, au sens du paragraphe 2(1) de la Loi réglementant certaines drogues et autres substances, dont la vente ou la fourniture ne nécessite pas d'ordonnance en vertu de cette loi;
- c) un médicament à l'égard duquel un avis de conformité a été délivré d'après les renseignements et le matériel contenus dans la présentation déposée conformément à l'article C.08.002.1 du Règlement sur les aliments et drogues;
- d) un médicament destiné à l'usage vétérinaire.
(3) Les alinéas 4(4)a) et b) du même règlement sont remplacés par ce qui suit :
- a) le prix obtenu par le titulaire de brevet, compte tenu des ajustements apportés par le titulaire ou toute partie qui directement ou indirectement achète le médicament ou rembourse pour l'achat de celui-ci et de toute déduction accordée à toute partie sous forme de biens ou services gratuits, cadeaux ou autres avantages semblables, doit être utilisé pour le calcul du prix moyen par emballage dans lequel le médicament était vendu;
- b) le montant des recettes obtenues par le titulaire de brevet, compte tenu des ajustements apportés par le titulaire ou toute partie qui directement ou indirectement achète le médicament ou rembourse pour l'achat de celui-ci et de toute déduction accordée à toute partie sous forme de biens ou services gratuits, cadeaux ou autres avantages semblables, doit être utilisé pour le calcul des recettes nettes pour chaque forme posologique, chaque concentration et chaque format d'emballage dans lesquels le médicament était vendu sous sa forme posologique finale.
3 Le même règlement est modifié par adjonction, après l'article 4, de ce qui suit :
4.1 (1) Pour l'application des alinéas 80(1)d) et (2)d) de la Loi, les renseignements à fournir à l'égard du facteur prévu à l'alinéa 4.4a) sont toutes les analyses coût-utilité préparées par un organisme canadien financé par l'État, si elles sont publiées, dont les résultats sont exprimés en fonction du coût par année de vie pondéré par la qualité, pour chaque indication faisant l'objet de l'analyse.
(2) Les renseignements visés au paragraphe (1) doivent être fournis :
- a) si les renseignements sont publiés au moment où le médicament est offert en vente au Canada pour la première fois, dans les trente jours suivant le jour où il est offert en vente au Canada pour la première fois;
- b) si les renseignements ne sont pas publiés au moment où le médicament est offert en vente au Canada pour la première fois, dans les trente jours suivant leur publication.
(3) Malgré le paragraphe (2), s'agissant des médicaments offerts en vente au Canada avant le 1er janvier 2019, les renseignements visés au paragraphe (1) doivent être fournis :
- a) si les renseignements sont publiés avant le 1er janvier 2019, au plus tard le 30 janvier 2019;
- b) si les renseignements ne sont pas publiés avant le 1er janvier 2019, dans les trente jours suivant leur publication.
(4) Toute autre analyse — telle que celle décrite au paragraphe (1) — publiée après que celles visées à ce paragraphe ont été fournies doit être fournie dans les trente jours suivant sa publication.
4.2 (1) Pour l'application des alinéas 80(1)d) et (2)d) de la Loi, les renseignements à fournir concernant le facteur prévu à l'alinéa 4.4b) sont l'utilisation maximale approximative du médicament au Canada, en fonction de la quantité prévue des ventes du médicament dans sa forme posologique finale, pour chaque forme posologique et chaque concentration dans lesquels le médicament devrait être vendu.
(2) Les renseignements visés au paragraphe (1) doivent être fournis dans les trente jours suivant le jour où le médicament est offert en vente au Canada pour la première fois.
(3) Malgré le paragraphe (2), s'agissant d'un médicament offert en vente au Canada avant le 1er janvier 2019, la version la plus récente des renseignements visés au paragraphe (1) doit être fournie :
- a) si le médicament est offert en vente au Canada pour la première fois pendant la période commençant le 1er janvier 2016 et se terminant le 31 décembre 2018, au plus tard le 30 janvier 2019;
- b) si les renseignements visés au paragraphe (1) à l'égard du médicament n'ont pas à être fournis aux termes de l'alinéa a) mais font l'objet d'une mise à jour :
- (i) pendant la période commençant le 1er janvier 2016 et se terminant le 31 décembre 2018, au plus tard le 30 janvier 2019,
- (ii) après le 31 décembre 2018, dans les trente jours suivant la mise à jour.
(4) Les renseignement fournis en vertu du présent article doivent être tenus à jour, et toute modification qui leur est apportée doit être présentée dans les trente jours suivant celle-ci.
4.3 (1) Malgré les paragraphes 4.1(2) et (3) et 4.2(2) et (3), s'agissant des médicaments ci-après, les renseignements visés aux paragraphes 4.1(1) et 4.2(1) doivent être fournis au Conseil, dans les trente jours suivant l'envoi, par ce dernier, d'une demande visant à ce que le breveté fournisse ces renseignements :
- a) un médicament qui n'est pas une drogue sur ordonnance au sens de l'article A.01.010 du Règlement sur les aliments et drogues;
- b) un médicament qui contient une substance désignée, au sens du paragraphe 2(1) de la Loi réglementant certaines drogues et autres substances, dont la vente ou la fourniture ne nécessite pas d'ordonnance en vertu de cette loi;
- c) un médicament à l'égard duquel un avis de conformité a été délivré d'après les renseignements et le matériel contenus dans la présentation déposée conformément à l'article C.08.002.1 du Règlement sur les aliments et drogues;
- d) un médicament destiné à l'usage vétérinaire.
(2) Les exigences des paragraphes 4.1(4) et 4.2(4) s'appliquent à l'égard des renseignements fournis en application du paragraphe (1).
Autres facteurs à considérer — prix excessifs
4.4 Pour l'application de l'alinéa 85(1)e) de la Loi, les autres facteurs dont le Conseil doit tenir en compte pour décider si le prix d'un médicament vendu après le 31 décembre 2018 sur un marché canadien est excessif sont les suivants :
- a) la valeur pharmacoéconomique du médicament au Canada et celle d'autres médicaments de la même catégorie thérapeutique;
- b) la taille du marché de ce médicament au Canada et dans d'autres pays que le Canada;
- c) le produit intérieur brut au Canada et le produit intérieur brut par habitant au Canada.
4 L'annexe du même règlement est remplacée par l'annexe figurant à l'annexe du présent règlement.
Entrée en vigueur
5 Le présent règlement entre en vigueur le 1er janvier 2019.
ANNEXE
(article 4)
ANNEXE
(sous-alinéa 4(1)f)(iii))
- Allemagne
Germany - Australie
Australia - Belgique
Belgium - Espagne
Spain - France
France - Italie
Italy - Japon
Japan - Norvège
Norway - Pays-Bas
Netherlands - République de Corée
Republic of Korea - Royaume-Uni
United Kingdom - Suède
Sweden
[48-1-o]